|
i, что подтверждает роль мобильных Са2+ буферов с низким
молекулярным весом в эффективном регулировании внутриклеточной концентрации
кальция.
2.1.3 Кальциевые каналы эндоплазматического ретикулума
Са2+ каналы ЭР являются олигометрическими протеинами, встроенными в
мембрану ЭР. Эти каналы можно относительно легко выделить из клетки для
дальнейшего структурного анализа благодаря тому, что белки канала связываются
специфически и с высоким сродством с IP3 (для IP3
-управляемых каналов) и с рианодином (для Са2+-управляемых каналов).
Са2+-управляемые Са2+ каналы ЭР. Эти кальциевые
каналы были впервые выделены из скелетных и сердечных мышц. Оказалось, что Са
2+ каналы ЭР в этих мышечных тканях имеют молекулярные различия и
закодированы различными генами. Са2+ каналы ЭР в сердечных мышцах
непосредственно связаны с высокопороговыми Са2+ каналами плазмалеммы
(L-тип) через кальцийсвязывающие белки, образуя, таким образом, функционально
активную структуру - «триаду». В скелетных мышцах деполяризация плазмалеммы
прямо активирует освобождение Са2+ из саркоплазматического
ретикулума благодаря тому, что Са2+ каналы плазмалеммы служат
потенциал - чувствительными передатчиками активирующего сигнала непосредственно
Са2+ каналам ЭР через связывающие белки (44). Таким образом, Са
2+ депо скелетных мышц обладают механизмом освобождения Са2+,
вызываемым деполяризацией (RyR1-тип). В отличие от скелетных мышц,
саркоплазматические Са2+ каналы кардиомиоцитов не связаны с
плазмалеммой, и для стимуляции освобождения Са2+ из депо требуется
увеличение концентрации цитозольного кальция (RyR2-тип). ДНК, кодирующая белки
двух типов каналов Са2+ освобождения, была клонирована из тканей
человека и кролика, что дало возможность экспрессировать Са2+
-управляемые Са2+ каналы в модельные клеточные системы. Белки,
встроенные в липидный бислой, формируют чувствительные к рианодину каналы,
активируемые ионами Са2+ (50 нмоль/л) в присутствии АТФ (29). Кроме
этих двух типов Са2+-активируемых Са2+ каналов, недавно
был идентифицирован третий тип Са2+ каналов ЭР (RyR3-тип), который
является продуктом другого гена. Этот третий тип Са2+ каналов ЭР,
как было показано, не чувствителен к кофеину (21). Эксперименты, проведенные на
нервных тканях, продемонстрировали присутствие всех трех типов Са2+
-управляемых Са2+ каналов ЭР в мозге млекопитающих, однако RyR2-тип
является доминантным (38). Са2+-управляемые Са2+ каналы
ЭР являются гомотетрамерами, состоящими из мономеров с молекулярным весом 500
КД (39)
IP3-управляемые Са2+ каналы ЭР. Существование IP
3-управляемых Са2+ каналов впервые было обнаружено в нейронах
Пуркинье. Позже было показано, что они встроены в мембрану эндоплазматического
ретикулума. Структура IP3-управляемых Са2+ каналов сходна
со структурой Са2+-управляемых Са2+ каналов ЭР. Они также
являются гомотетрамерами с молекулярным весом мономера 260 КД. 50% этих каналов
активируется 15 мкмоль/л IP3 и блокируется рутением красным и La
3+. IP3-управляемые Са2+ каналы были выделены из
мозга млекопитающих, и их аминокислотная последовательность была расшифрована.
Было показано, что семейство генов, экспрессирующих IP3-управляемые
Са2+ каналы, состоит из трех или четырех различных генов; они
характеризуются различной чувствительностью к IP3 и по-разному
распределены в мозге млекопитающих (45). Порог активации этих каналов варьирует
между 0.2 - 0.5 мкмоль/л в нейронах Пуркинье мозжечка и возрастает до 9
мкмоль/л в астроцитах.
2.1.4 Кальциевые насосы
Существует два семейства Са2+ насосов, ответственных за устранение
ионов Са2+ из цитоплазмы: Са2+ насосы плазмалеммы и Са
2+ насосы эндоплазматического ретикулума. Хотя они относятся к одному
семейству белков (так называемому P-классу АТФ-аз), эти насосы обнаруживают
некоторые различия в строении, функциональной активности и фармакологии.
Кальциевый насос плазмалеммы. Са2+ насос плазмалеммы, который
удаляет ионы Са2+ из цитоплазмы в межклеточное пространство, был
открыт в 1966 году. Молекулярные свойства Са2+ насосов плазмалеммы
описаны в нескольких обзорах (18), однако достоверных данных о скорости вывода
Са2+ и регуляции Са2+ насосов в нервных клетках немного.
Недавно был разработан двухфлуоресцентный микрокапельный метод (58),
позволяющий одновременно измерять [Ca2+]i и выход Са
2+ наружу на одиночных клетках. Исследования, проведенные с помощью
данного метода на нейронах моллюска и секреторных клетках, показали, что
активность Са2+ насоса плазмалеммы контролируется непосредственно
[Ca2+]i: увеличение концентрации цитоплазматического
кальция активирует Са2+ насос (58). В нейронах моллюска около 40%
ионов кальция, входящих в клетку в ответ на деполяризацию мембраны, выводится
из нейрона уже во время фазы нарастания [Ca2+]i, отражая
таким образом активацию кальциевого насоса плазмалеммы увеличением концентрации
цитозольного Са2+ (58).
Кальциевый насос эндоплазматического ретикулума. Во многих
эукариотических клетках, наряду с Са2+ насосом плазмалеммы,
существует кальциевый насос сарко(эндо)плазматического ретикулума (SERCA). В
настоящее время описано по крайней мере 3 различных изоформы SERCA-насосов в
клетках млекопитающих. SERCA1-подтип сосредоточен исключительно в быстрых
скелетных мышцах, SERCA2-насосы широко распространены в других тканях.
Значимость SERCA3-насосов менее ясна (13). Белки SERCA2-насосов разделяются на
две различные изоформы: SERCA2а, характерные для кардиомиоцитов и гладких мышц,
и SERCA2b, характерные для тканей мозга. Предполагается, что насосы SERCA
различными способами регулируются цитоплазматической и интралюминальной
концентрациями Са2+: Увеличение [Ca2+]i
активирует захват ионов кальция в ЭР, в то время как увеличение свободного
кальция внутри ЭР ингибирует насосы SERCA (12). Насосы SERCA эффективно и
селективно блокируются тапсигаргином в наномолярных концентрациях (37) и
микромолярными концентрациями циклопиазоновой кислоты. Однако, тапсигаргин
вызывает также блокаду потенциал - управляемых кальциевых каналов плазмалеммы,
как это показано на клетках коркового слоя надпочечников и на сенсорных
нейронах (Shmigol et al., 1995), поэтому его следует использовать с
некоторой осторожностью.
2.1.5 Кальциевые обменники
Дополнительным механизмом, ответственным за вывод ионов кальция из цитоплазмы,
является натрий-кальциевый обменник, который выводит Са2+, используя
энергию натриевого электрохимического градиента. Наличие Na+- Са
2+ обменника было показано в различных типах возбудимых и невозбудимых
клеток; в клетках нервной системы он был обнаружен в конце 60-х годов (9). В
нейронах моллюска, помещенных в среду с пониженным натрием (т.е. с обратным
натриевым градиентом), наблюдалось увеличение [Ca2+]i,
что является результатом работы обменника в инвертированной форме. Однако,
вклад Na+- Са2+ обменника в регуляцию [Ca2+]
i в нейронах млекопитающих до сих пор не оценен. В некоторых работах было
показано, что обменник принимает незначительное участие в удалении
цитоплазматического Са2+, в то время как в других работах
представлены данные о том, что обменник играет существенную роль в переносе Са
2+ через мембрану (57).
2.1.6 Са2+-связывающие органеллы
Кроме быстрого связывания цитозольного Са2+ внутриклеточными Са
2+-связывающими белками, ионы кальция, попадающие в цитозоль, могут
аккумулироваться аппаратом Гольджи или клеточным ядром, захватываться
митохондриальными Са2+ депо, имеющими достаточно невысокое сродство
к Са2+, или быстрыми депо, связанными с ЭР или СР, имеющими высокое
сродство к Са2+. Однако если [Ca2+]i превышает
0,5 мкмоль/л, наблюдается существенное перераспределение [Ca2+]
i в область митохондрий. Буферные системы митохондрий принимают участие в
удалении избыточного Са2+ из цитоплазмы в клетках кишечника,
некоторых типах нервных клеток (59) и в секреторных клетках после повышения [Ca
2+]i, стимулированного агонистами. Связывание кальция
митохондриями обеспечивается активностью систем, расположенных на внутренней
митохондриальной мембране. Са2+ поступает в митохондрии по
электрохимическому градиенту; разность потенциалов, обеспечивающая транспорт
кальция, создается переносом электронов во время клеточного дыхания и
связанного с ним переносом протонов. Перенос электронов по дыхательной цепи
является основным механизмом, обеспечивающим энергетику транспорта кальция.
Подавление дыхательной цепи карбонил-цианид-м-хлорофенил-гидразоном (СССР)
эффективно блокирует аккумуляцию кальция митохондриями (41).
2.2 Влияние АТФ на кальциевый гомеостаз
Последние исследования показали, что АТФ занимает прочное место в ряду
нейромедиаторов центральной и периферической нервной систем (Burnstock 1990).
Не вызывает сомнения, что АТФ является не только важнейшим внутриклеточным
метаболитом, но и служит важным объектом межклеточного взаимодействия.
2.2.1 Строение и свойства АТФ
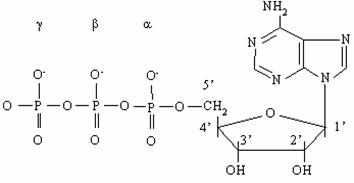
| Рисунок 1. Строение молекулы АТФ |
|
|
АТФ (см. рис.1) представляет собой нуклеотид и как всякий нуклеотид состоит
из трех компонентов: азотистого основания, сахара пентозы и фосфата. В
качестве азотистого основания в нуклеотидах присутствуют производные пурина и
пиримидина. Фосфаты соединены в полифосфатную цепь, количество которых в
естественных нуклеотидах не превышает трех. Однако синтезированы нуклеотиды,
содержащие линейные цепи из более чем 3-х фосфатов, к примеру аденозинтетра-
и аденозинпентафосфаты.
Названия нуклеотидов, содержащих в качестве сахара рибозу, складываются из
названия соответствующего нуклеозида, приставки, обозначающей количество
фосфатных групп в нуклеотиде и слова фосфат. Для наиболее распространенных
нуклеотидов приняты сокращенные названия, например АТФ для
аденозинтрифосфата, ГТФ - для гуанозинтрифосфата, ИМФ - инозинмонофосфата.
В области нейтральных значений pH нуклеиновые основания и рибоза в растворе не
заряжены (Мартин, Мариам, 1982). Нуклеотиды, из-за наличия фосфатов,
представляют собой сильные кислоты. АТФ содержит четыре ОН группы, способные к
ионизации, три из которых имеют pKa ниже 3, а pKa четвертой - 6,5 (Ленинджер,
1976). Таким образом, при pH 7,4 подавляющее большинство молекул АТФ
представляют собой четырехзарядные анионы АТФ4- , кроме того, в
растворе присутствует небольшое количество АТФ3-.
2.2.2 Номенклатура и субклассификация пуринорецепторов.
Первое разделение пуринорецепторов на Р1 и Р2 типы
основывалось на следующем критерии: нуклеозиды такие как аденозин активировали
Р1 пуринорецепторы, в то время как АТФ стимулировала Р2
пуринорецепторы, а метилксантины (кофеин, теофиллин) являются селективными
антагонистами Р1 пуринорецепторов. Также Р1
пуринорецепторы связаны с аденилатциклазой, а активация Р2
пуринорецепторов может приводить к выработке простогландинов (Burnstock 1978).
2.2.3 Р1 пуринорецепторы.
В 1979 году (Van Calker et al 1979) показали, что аденозиновые, Ð1
- пуринорецепторы можно подразделить на две группы. Рецепторы одной из них
обладали очень высоким сродством к аденозину (константа диссоциации Кd
= 3 - 10 нМ). При взаимодействии аденозина с этой группой рецепторов наблюдалось
ингибирование аденилатциклазы и, следовательно, уменьшался уровень
внутриклеточного цАМФ. Этот класс рецепторов был назван А1
-рецепторами (Ri рецепторы по (Londos et al 1980)). Аденозиновые
рецепторы, относящиеся ко второй группе, имели более низкое сродство к
аденозину (Кd комплекса аденозина с рецептором 5-10 мкМ). Активация
этого типа рецепторов приводила к стимуляции аценилатциклазы. Эти рецепторы Ван
Колкер назвал А2-рецепторами (Ra рецепторы по (Londos et
al 1980)). Были обнаружены также и мощные антагонисты для А1 - R-N
6-Фенилизопропиладенозин (R-PIA). Для А2 более сильным
антагонистом был 5’-N-этилкарбоксамидаденозин (NЕСА). Также существуют работы,
в которых описываются аденозиновые рецепторы, не связанные с аденилатциклазой
эти пуринорецепторы было предложено назвать А3 (Ribeiro and
Sebastiao 1986). Предпосылкой к разделению А2 пуринорецепторов на А
2а и А2b подтипы стало открытие разного сродства
Страницы: 1, 2, 3, 4, 5
|

