|
Меню
|
 |
|
|
|
|
|
|

|
Курсовая: Содержание аскорбиновой, дегидроаскорбиновой и дикетогулоновой кислот в эритроцитах здоровых детей и страдающих инсулинзависимым сахарным диабетом
|
 |
|
ние имеет место в организме (Халмурадов, Тоцкий, 1993):
Способность к О-В превращениям, связанная с ендольной группировкой, которая
стабилизирована находящейся в цикле соседней карбонильной группировкой,
сопровождающаяся перенесением атомов водорода к акцепторам, является важнейшей
каталитической функцией АК в живом организме. L-АК по своей биологической
активности высокоспецифична. Витаминная активность проявляется только при
наличии свободных гидроксильных групп. Различные функциональные производные по
ним лишают молекулу витаминной активности почти полностью, как и гидрирование
ненасыщенной связи лактонного кольца. Поэтому L-ДАК имеет витаминную
активность, равноценную L-АК, тогда как 2,3-ДКГК полностью ее лишена.
Вследствие легкой окисляемости L-АК – донор Н+, она количественно
легко восстанавливает многочисленные соединения, как-то: йод, перманганат калия
и другие. L-АК – переносчик Н+ в некоторых ферментативных реакциях
живой клетки, она легко окисляется пероксидазой, цитохромоксидазой, каталазой.
L-АК восстанавливает окисленные формы ферментов, окисляясь в ДАК, обратимо
легко регенерирующуюся в АК под действием глутатиона за счет его
сульфгидрильной группы:
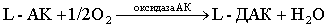
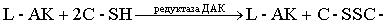
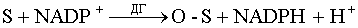
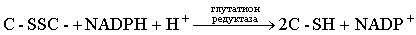 Окисление АК катализируется медью, в меньшей степени – катионами серебра и
железа. Имеется предположение, что специфическим катализатором окисления АК в
животных организмах является белок, синтезирующийся в печени, осуществляющий
транспорт меди, обладающий оксигеназной активностью, - церулоплазмин. В меньшей
степени окисление аскорбата катализируют другие катионы, в частности, серебра и
железа. Комплексоны, флавоноиды тормозят окислительный распад АК. Некоторые
белки ингибируют окисление АК, связываясь с ней или путём образования комплекса
с медью – сывороточные глобулины (Борец, 1980). Окисление тормозится –SH
содержащими соединениями: сернистая кислота блокирует фермент аскорбиназу; С-SH
связывает ионы Cu+, удаляя т. с. катализатор окисления АК из реакции
(Киверин, 1971).
1.2.2. Биосинтез АК в живом организме
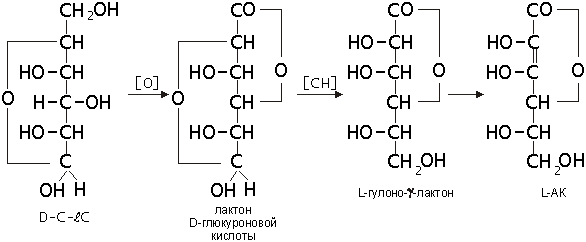
L-АК синтезируется в растениях и организме некоторых животных из D-глюкозы
через лактон D-глюкуроновой кислоты и L-гулоно-γ-лактон или их
производное. В процессе биосинтеза происходит превращение соединений D-ряда в
соединения L-ряда (Березовский, 1993):
Биосинтез АК в организме животных происходит в клетках печени, почек,
надпочечников, гипофиза, стенки тонкого кишечника (Киварин, 1973).
1.2.3. Физиологические свойства аскорбата
Витамин С является постоянной составной частью тканей и органов человека. Его
поступление в организм должно быть ежедневным, т. к. аскорбат, играя важную
роль в обменных процессах организма, все время расходуется. Он
восстанавливает окисленные формы ферментов, активирует некоторые протеазы,
тормозит действие амилазы и протеазы поджелудочной железы, активирует
эстеразу печени. L-АК участвует в обмене некоторых ароматических аминокислот,
регулирует уровень холестерина в крови, усиливает антитоксические функции
гепатоцитов (вкупе с глюкозой), норамализирует белковообразование. Витамин С
необходим для нормального функционирования клеток, продуцирующих коллаген,
активирует и регулирует зритропоэз (способствуя усвоению железа), нормализует
нарушенное протромбинообразование, нормализует процессы свертывания (Андреев;
1996). Аскорбат играет положительную роль в развитии иммунных реакций
организма, обладает некоторым детоксицирующим свойством, является
существенным фактором профилактики и лечения инфекционных заболеваний.
Витамин С оказывает положительное воздействие на углеводный обмен. Волынский
З. М. с сотрудниками показали, что повышает синтез гликогена в печени, и что
нарастание содержания гликогена в печени, как правило, прямо пропорционально
повышению в этом органе витамина С. К такому выводу позволяют прийти
многочисленные клинические наблюдения последнего времени, подтверждающие
ценное свойство АК обладать нормализующим действием на уровень сахара в
крови. Подобный эффект связан с синергическим действием аскорбата и гормонов
– инсулина и адреналина. Витамин С может усиливать действие инсулина или
действовать аналогично ему, способствуя образование гликогена в печени.
Синергизм возникает косвенным путем через воздействие инсулина и витамина С
на общегормональный фон организма.
Таким образом, АК оказывает разностороннее влияние на процессы обмена веществ
у здоровых людей, а при различных патологических состояниях благоприятствует
нормальному течению обмена веществ и функционированию различных органов и
систем организма (Бременер; 1997).
1.3. Сахарный диабет как один из распространенных патологических процессов
Диабет сахарный (diabetes mellitus; сахарная болезнь, сахарное мочеизнурение)
– эндокринное заболевание, обусловленное дефицитом гормона инсулина в
организме или его низкой биологической активностью; характеризуется
хроническим течением, нарушением всех видов обмена веществ, ангиопатией.
Сахарный диабет представляет собой самую распространённую эндокринную
патологию. В его развитии существенную роль играют наследственная
предрасположенность и неблагоприятное воздействие окружающей среды, однако,
характер наследственной предрасположенности и так называемых факторов риска
различны при разных типах сахарного диабета. Факторами риска развития
сахарного диабета являются появление антител к b-клеткам островков
поджелудочной железы, частые вирусные инфекции, гиподинамия, ожирение,
нерациональное или недостаточное питание, стрессы, генетически отягощенный по
сахарному диабету анамнез и другие.
Согласно классификации ВОЗ, различают два основных типа сахарного диабета.
Это инсулинзависимый (I тип) и инсулиннезависимый (II тип) сахарный диабет.
Инсулинзависимый сахарный диабет, как правило, развивается у лиц молодого
возраста и детей, имеющих генетическую предрасположенность к сахарному
диабету именно данного типа. Инсулиннезависимым сахарным диабетом чаще болеют
лица, старше 50 лет (особенно женщины). Наследственная предрасположенность
играет большую роль, чем при сахарном диабете I – типа.
Механизм развития сахарного диабета сложен и многогранен. Он зависит как от
функции самой поджелудочной железы, так и от внепанкреатических факторов.
Прежде всего, нарушен обмен углеводов. Из-за недостатка инсулина или других
причин затрудняется переход глюкозы в мышечную и жировую ткань, снижается
синтез гликогена в печени, усиливается образование глюкозы из белков и жиров
(глюконеогенез). В развитии этих процессов увеличивается содержание глюкозы в
крови. Если в норме оно довольно устойчиво и натощак у здоровых людей
колеблется в пределах 3,33 – 35,55 ммоль/л (70 – 100 мг%), то при сахарном
диабете в зависимости от формы и тяжести течения обычно превышает 6,00
ммоль/л, достигая 20 –30 ммоль/л и больше.
Диабет у детей и подростков характеризуется тяжелым течением и, как правило,
острым началом заболевания. От времени появления первых признаков заболевания
(жажда, похудание, выделение большого количества мочи, общая слабость,
сухость кожи) до развития тяжёлого состояния и значительных нарушений обмена
веществ, проходит обычно 2 недели. Дети, больные сахарным диабетом, требуют
обязательного лечения и постоянного лечебного контроля.
Окисление АК катализируется медью, в меньшей степени – катионами серебра и
железа. Имеется предположение, что специфическим катализатором окисления АК в
животных организмах является белок, синтезирующийся в печени, осуществляющий
транспорт меди, обладающий оксигеназной активностью, - церулоплазмин. В меньшей
степени окисление аскорбата катализируют другие катионы, в частности, серебра и
железа. Комплексоны, флавоноиды тормозят окислительный распад АК. Некоторые
белки ингибируют окисление АК, связываясь с ней или путём образования комплекса
с медью – сывороточные глобулины (Борец, 1980). Окисление тормозится –SH
содержащими соединениями: сернистая кислота блокирует фермент аскорбиназу; С-SH
связывает ионы Cu+, удаляя т. с. катализатор окисления АК из реакции
(Киверин, 1971).
1.2.2. Биосинтез АК в живом организме
L-АК синтезируется в растениях и организме некоторых животных из D-глюкозы
через лактон D-глюкуроновой кислоты и L-гулоно-γ-лактон или их
производное. В процессе биосинтеза происходит превращение соединений D-ряда в
соединения L-ряда (Березовский, 1993):
Биосинтез АК в организме животных происходит в клетках печени, почек,
надпочечников, гипофиза, стенки тонкого кишечника (Киварин, 1973).
1.2.3. Физиологические свойства аскорбата
Витамин С является постоянной составной частью тканей и органов человека. Его
поступление в организм должно быть ежедневным, т. к. аскорбат, играя важную
роль в обменных процессах организма, все время расходуется. Он
восстанавливает окисленные формы ферментов, активирует некоторые протеазы,
тормозит действие амилазы и протеазы поджелудочной железы, активирует
эстеразу печени. L-АК участвует в обмене некоторых ароматических аминокислот,
регулирует уровень холестерина в крови, усиливает антитоксические функции
гепатоцитов (вкупе с глюкозой), норамализирует белковообразование. Витамин С
необходим для нормального функционирования клеток, продуцирующих коллаген,
активирует и регулирует зритропоэз (способствуя усвоению железа), нормализует
нарушенное протромбинообразование, нормализует процессы свертывания (Андреев;
1996). Аскорбат играет положительную роль в развитии иммунных реакций
организма, обладает некоторым детоксицирующим свойством, является
существенным фактором профилактики и лечения инфекционных заболеваний.
Витамин С оказывает положительное воздействие на углеводный обмен. Волынский
З. М. с сотрудниками показали, что повышает синтез гликогена в печени, и что
нарастание содержания гликогена в печени, как правило, прямо пропорционально
повышению в этом органе витамина С. К такому выводу позволяют прийти
многочисленные клинические наблюдения последнего времени, подтверждающие
ценное свойство АК обладать нормализующим действием на уровень сахара в
крови. Подобный эффект связан с синергическим действием аскорбата и гормонов
– инсулина и адреналина. Витамин С может усиливать действие инсулина или
действовать аналогично ему, способствуя образование гликогена в печени.
Синергизм возникает косвенным путем через воздействие инсулина и витамина С
на общегормональный фон организма.
Таким образом, АК оказывает разностороннее влияние на процессы обмена веществ
у здоровых людей, а при различных патологических состояниях благоприятствует
нормальному течению обмена веществ и функционированию различных органов и
систем организма (Бременер; 1997).
1.3. Сахарный диабет как один из распространенных патологических процессов
Диабет сахарный (diabetes mellitus; сахарная болезнь, сахарное мочеизнурение)
– эндокринное заболевание, обусловленное дефицитом гормона инсулина в
организме или его низкой биологической активностью; характеризуется
хроническим течением, нарушением всех видов обмена веществ, ангиопатией.
Сахарный диабет представляет собой самую распространённую эндокринную
патологию. В его развитии существенную роль играют наследственная
предрасположенность и неблагоприятное воздействие окружающей среды, однако,
характер наследственной предрасположенности и так называемых факторов риска
различны при разных типах сахарного диабета. Факторами риска развития
сахарного диабета являются появление антител к b-клеткам островков
поджелудочной железы, частые вирусные инфекции, гиподинамия, ожирение,
нерациональное или недостаточное питание, стрессы, генетически отягощенный по
сахарному диабету анамнез и другие.
Согласно классификации ВОЗ, различают два основных типа сахарного диабета.
Это инсулинзависимый (I тип) и инсулиннезависимый (II тип) сахарный диабет.
Инсулинзависимый сахарный диабет, как правило, развивается у лиц молодого
возраста и детей, имеющих генетическую предрасположенность к сахарному
диабету именно данного типа. Инсулиннезависимым сахарным диабетом чаще болеют
лица, старше 50 лет (особенно женщины). Наследственная предрасположенность
играет большую роль, чем при сахарном диабете I – типа.
Механизм развития сахарного диабета сложен и многогранен. Он зависит как от
функции самой поджелудочной железы, так и от внепанкреатических факторов.
Прежде всего, нарушен обмен углеводов. Из-за недостатка инсулина или других
причин затрудняется переход глюкозы в мышечную и жировую ткань, снижается
синтез гликогена в печени, усиливается образование глюкозы из белков и жиров
(глюконеогенез). В развитии этих процессов увеличивается содержание глюкозы в
крови. Если в норме оно довольно устойчиво и натощак у здоровых людей
колеблется в пределах 3,33 – 35,55 ммоль/л (70 – 100 мг%), то при сахарном
диабете в зависимости от формы и тяжести течения обычно превышает 6,00
ммоль/л, достигая 20 –30 ммоль/л и больше.
Диабет у детей и подростков характеризуется тяжелым течением и, как правило,
острым началом заболевания. От времени появления первых признаков заболевания
(жажда, похудание, выделение большого количества мочи, общая слабость,
сухость кожи) до развития тяжёлого состояния и значительных нарушений обмена
веществ, проходит обычно 2 недели. Дети, больные сахарным диабетом, требуют
обязательного лечения и постоянного лечебного контроля.
ГЛАВА 2. МАТЕРИАЛЫ И МЕТОДЫ
Нами обследован 41 ребёнок, страдающий инсулинзависимым сахарным диабетом, и
10 человек контрольной группы. Объектом исследования служили эритроциты
больных и здоровых детей. Для получения эритроцитов кровь брали из локтевой
вены капельным способом, в качестве антикоагулянта использовали гепарин.
Исследования проводили в общей эритроцитарной массе детей, страдающих
инсулинзависимым сахарным диабетом, и детей контрольной группы.
2.1. Подготовка эритроцитов
Свежую гепаринизированную кровь разливали в центрифужные пробирки по 5 мл. После
пятнадцатиминутного центрифугирования при 3000 об/мин при 40 С
отбирались и отбрасывались лейкоцитарный слой и плазма. Эритроциты
суспендировали в десятикратном объёме 0.9% раствора NaCl и центрифугировали в
течение пятнадцати минут при 3000 об/мин. Супернатант отсасывали, процедуру
повторяли 3 раза. Это делалось для более плотной упаковки эритроцитов.
2.2. Метод раздельного определения аскорбиновой, дегидроаскорбиновой и
дикетогулоновой кислот в эритроцитах
Для количественных определений АК, ДАК и ДКГК использовали метод J.H. Roe,
C.A. Kuether (1943) в модификации В.В. Соколовского, Л.В. Лебедевой, Т.Б.
Лиэлуп (1967). Метод основан на взаимодействии 2,4- динитрофенилгидразина с
ДАК с образованием в серной кислоте соответствующего озазона. ДАК и ДКГК дают
красное окрашивание, используемое для фотометрического определения. Для
вычисления суммы всех кислот их окисляют 2,6- дихлорфенолиндофенолятом
натрия. Содержание АК определяют по разности. Для дифференцированного
определения ДАК и ДКГК смесь подвергают действию восстановителей, при этом в
АК восстанавливается только ДАК. В качестве восстановителя использовали
димеркаптопропансульфонат натрия (унитиол)
Реактивы:
1. 2.10 М унитиол (0.84 мл 5% раствора ампулированного препарат
в 100 мл 0.2 М фосфатного буфера рН 7.0. хранить не более суток).
2. 5% трихлоруксусная кислота (ТХУ). Хранить в холодильнике не более
двух недель.
3. 85% раствор серной кислоты (100 мл воды + 900 мл концентрированной
серной кислоты).
4. 2% раствор 2,4-динитрофенилгидразина в 9Н серной кислоте, содержащей
0.25% тиомочевины (хранить в холодильнике не более 1 месяца).
5. 0.001 Н раствор 2,6- дихлорфенолиндофенолята натрия (краска
Тильманса). Хранить в темноте не более 1 недели.
6. 0.9% раствор хлорида натрия (физиологический раствор).
Ход определения.
В три пробирки помещали по 0.5 мл упакованных и отмытых от плазмы эритроцитов
с известным гематокритом. В первую прибавляли 0.25 мл физиологического
раствора и 0.25 мл унитиола. После пятнадцатиминутной инкубации при
периодическом помешивании суспензии отбирали 0.5 мл экстракта, к которому
прибавляли 1.5 мл ТХУ.
В две другие пробирки также прибавляли по 1.5 мл ТХУ.
В две пробирки вносили по 0.75 мл супернатанта, полученного при
центрифугировании смеси упакованных эритроцитов с ТХУ. В одну из пробирок
добавляли по каплям 0.001 Н раствор 2,6- дихлорфенолиндофенолята натрия до
появления слаборозового окрашивания, устойчивого в течение 30 секунд. В третью
пробирку помещали 0.75 мл супернатанта, полученного после центрифугирования
смеси упакованных эритроцитов с физиологическим раствором, унитиолом и ТХУ. Во
все пробирки добавляли по 0.25 мл 2,4- динитрофенилгидразина и доводили объём
до 1.25 мл дистиллированной водой, инкубировали при 100 0 С в
течение 10 минут и охлаждали в ледяной бане. В каждую пробирку добавляли
небольшими порциями 1.25 мл 85% раствора серной кислоты, охлаждая в ледяной
бане после каждой порции. Окрашенные растворы фотометрировали через час при
длине волны 540 нм.
Концентрацию кислот определяли по формуле:
С = (3*А)/0.085; где
С – концентрация кислот, мг%
3 – концентрация стандартного раствора, мг%
А – оптическая плотность пробы
0.085 – оптическая плотность стандартного раствора
2.3. СТАТИСТИЧЕСКАЯ ОБРАБОТКА РЕЗУЛЬТАТОВ
Результаты исследований обрабатывались статистически (Лакин И.А., 1976).
Глава 3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Страницы: 1, 2, 3
|
|
|
|

|
НОВОСТИ
|

|
|
|
|
|
|
|